相比其它组学文章,单细胞文章有一特点,基于数据分析的图表结果特别丰富,也彰显了单细胞数据分析挖掘的重要性,如何利用数据处理+分析挖掘+基础实验验证,发表一篇10分+的文章,今天的文献解析你值得拥有~
标题:Integrated single-cell transcriptomic analyses reveal that GPNMB-high macrophages promote PN-MES transition and impede T cell activation in GBM
发表杂志:EBioMedicine(IF=11.205)
发表时间:202209
研究背景
胶质母细胞瘤(GBM)是具有侵袭性的原发性脑肿瘤类型,通常对目前的治疗具有耐药性,以肿瘤微环境为中心的疗法可能为GBM治疗带来新的希望。因此,迫切需要深入了解肿瘤-基质通讯,以确定有希望的治疗靶点。
研究方案设计
1、收集人、小鼠GBM的单细胞RNA测序(scRNA-seq)数据、RNA-seq数据和空间转录组(Spatial transcriptomics,ST)数据;
2、免疫细胞分选
1)小鼠脾脏T cells:EasySep Mouse T Cell Isolation Kit (Stemcell Technologies; 19851) ;
2)单核细胞:RPMI-1640 medium (Life Technologies, 11875119)冲洗股骨和胫骨,40μm滤器过滤,EasySep Mouse Monocytes Isolation Kit (Stemcell Technologies; 19861)分选.;
3)CD11b+F4/80+GPNMB+ macrophages and CD11c+MHCII+ dendritic cells:anti-CD45 (1:200, eBioscience), anti-CD11b (1:200, eBioscience), anti-CD11c(1:200, BioLegend), anti-F4/80 (1:200, BioLegend), anti-MHCII (1:200, eBioscience) and anti-GPNMB (1:100, Invitrogen)。
3、流式分选:小鼠GBM细胞悬液抗体孵育30 mins,anti-CD45 (1:200, eBioscience)、anti-CD3 (1:100, BioLegend)、anti-CD11b (1:200, BioLegend)、anti-CD11c (1:200, BioLegend)、anti-F4/80 (1:200, BioLegend)、anti-MHCII (1:200, eBioscience) 、IgG antibodies对照;
4、免疫荧光:anti-GPNMB (1:50, R&D Systems)、anti-Mac-3 (1:100, BD)、anti-CD3(1:100, Abcam) 。
5、细胞共培养:前神经元型胶质瘤细胞和新鲜分离的CD11b+ F4/80+巨噬细胞,每三天加入新鲜的巨噬细胞,持续的刺激后检测间充质表型的三种主要转录因子的表达(EPAS1、CEBPB、FOSL2)。
数据分析方法
1、scRNA-seq数据处理:Seurat,低质量细胞过滤(a cutoff value of less than 200 total feature RNA and more than 5% mitochondrial RNA)、SCTransform标准化、PCA降维(npcs=30)、细胞类群识别FindNeighbors and FindClusters(resolution=0.8)、差异分析FindAllMarkers function (cutoff:min.pct=0.25 and logfc.threshold=0.25);
2、ST数据处理:Seurat 4.0,SCTransform标准化、 PCA and UMAP降维聚类(npcs=30)、SpatialFeaturePlot空间可视化;
3、肿瘤拷贝数据变异:inferCNV,过滤expressed less than 10 cells and a median expression below 0.1;
4、细胞轨迹分析:Monocle 2,过滤expression was less than 0.5 and expressed cells were fewer than 200;
5、转录因子活性:SCIENCE,相关性GENIE3 (treeMethod= ”RF”, K=”sqrt”, nTrees?=?1000)
6、细胞通讯:Nichenet(Only the top 15% expressed genes in sender cells were calculated by regulatory potentials and ligand activity was ranked with a cutoff of 0.5 using Pearson test)、CytoTalk(分析T cells、 dendritic cells、Gpnmb-high macrophages、monocytes)
研究思路

研究结果
1、scRNA-seq分析GBM肿瘤异质性图谱
利用Seurat整合分析了来自不同数据集的scRNA-seq数据(GSE103224、GSE138794、GSE139448和GSE131928),共获得来自40例患者的54,534个细胞(图1a);利用inferCNV分析进一步鉴别肿瘤细胞和正常细胞(图1),与已发表的WES 数据一致;鉴定注释到的恶性细胞包括:MES-like细胞(12.2%,CHI3L1、ADM)、AC-like细胞(36%,MLC1、HOPX)、NPC-like细胞(4.9%,CD24、DCX)和OPC-like细胞(26.4%,PDGFRA、OLIG1),非肿瘤细胞包括:巨噬细胞(8.2%,CD163、CD68)、小胶质细胞(1.5%,CX3CR1、TMEM119)、淋巴细胞(0.7%,CD3D、NKG7)、内皮细胞(1.1%,VWF、PECAM1)、肿瘤相关内皮细胞(0.8%,COL1A2、BGN)、少突胶质细胞(4.3%,PTGDS、MBP)(图1c-d);GBM患者表现出高水平的瘤内异质性,尤其是肿瘤细胞(图1E-F);GSEA分析也验证了GBM的不同肿瘤细胞亚型(图1g)。
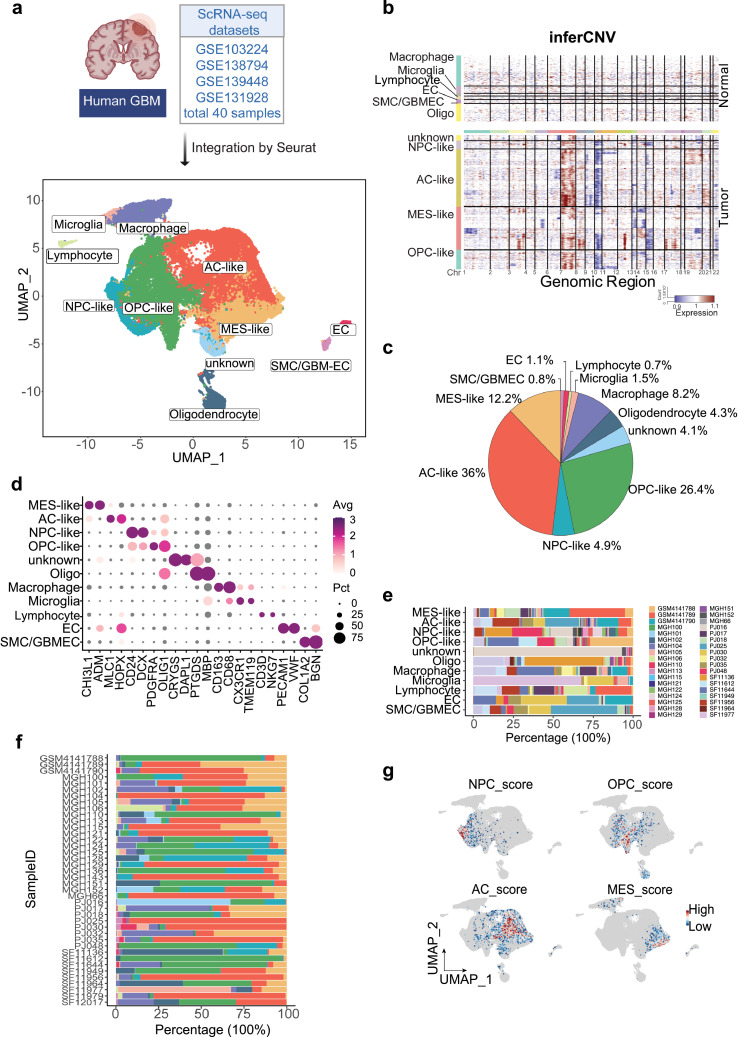
图1 scRNA-seq分析GBM肿瘤异质性图谱
2、轨迹分析揭示前神经元-间充质亚型转换中的关键转录调节因子
利用细胞轨迹分析,探索GBM不同肿瘤亚型间的分化关系,结果显示拟时间线上主要由NPC-和OPC-like 肿瘤细胞逐渐分化为AC-和MES-like肿瘤细胞,同时有个小分支为AC-like肿瘤细胞,揭示了GBM的可塑性和前神经元型(proneural, PN)到间质型(mesenchymal, MES)的动态过渡(图2a-c);PN与细胞周期、G2M检查点和神经胶质细胞分化相关的通路显著富集,表明PN具有高度增殖性和可塑性,而MES与上皮-间充质转化(EMT)、缺氧、ECM组织和细胞粘附相关的通路显著富集(图2d);利用TCGA数据集进行生存分析,结果显示,与PN组相比,具有MES-like转录组特征的患者总生存期较差,而与MES-low组相比,MES-high组预后更差,表明具有间充质特征的GBM患者的生存结局较差(图2e)。Tips:利用TCGA数据库中的临床数据,将单细胞数据中鉴定到关键maker基因或基因集进行生存分析,是探讨临床意义的有效途径。
利用SCENIC分析PN或MES细胞中的关键转录调控网络,结果显示,转录因子E2F1、SOX9、RARA、SOX11和SOX4在OPC和NPC细胞中差异过表达,而 EAPS1、CEBPB、FOSL2、STAT2和EGR1在MES和AC细胞状态中差异过表达,细胞轨迹分析证实了PN-MES转换过程中EPAS1、CEBPB和FOSL2的激活以及SOX4、SOX11的下调(图2k)。以上结果突出了从PN到MES细胞状态的动态转变主要是由关键转录因子驱动的。

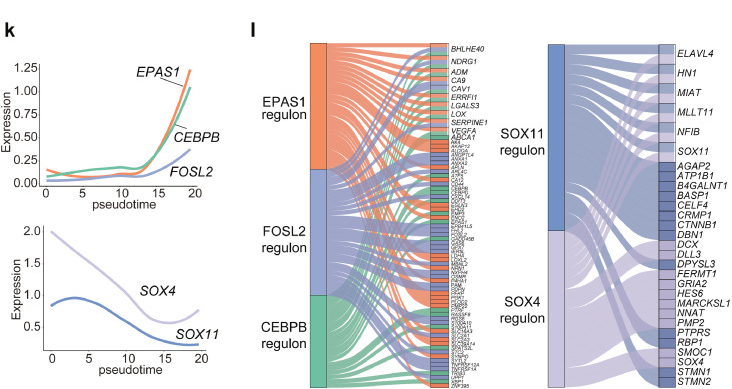
图2 轨迹分析揭示前神经元-间充质亚型转换中的关键转录调节因子
3、PN-和MES-GBM的肿瘤免疫微环境解析
利用MES基因特征将患者分为MES-high和MES-low组,发现MES-high组肿瘤微环境中伴有丰富的巨噬细胞、T细胞和内皮细胞浸润(图3a, b);但T细胞浸润在很多癌种的研究中与患者预后呈正相关,因此利用TCGA数据进一步分析,GBM MES亚型表达更高的T细胞和髓系细胞标志物,并且T细胞与巨噬细胞存在很强的相关性(图3c-d);对空间scRNA-seq数据进行分析,发现CD8 + T细胞与CD68 +髓系细胞、内皮细胞共定位(图3e),证实了T细胞与髓系细胞之间存在空间上的紧密接触,可能发生在血管微环境中(vascular niches)。Tips:每个实验组增加ST样本,不仅能与单细胞数据互相验证,还能对maker基因和细胞类型进行空间定位,精准锁定有真实空间物理接触的细胞间互作关系。
利用反卷积算法对TCGA数据进一步进行分析,发现T细胞丰度与巨噬细胞、树突状细胞显著相关,这是两个主要的髓系细胞(图3f);利用流式细胞术,分析小鼠GBM中的免疫细胞,证实了T细胞与CD11b + F480 +肿瘤相关巨噬细胞(TAM)或CD11c + MHCII + DC显著正相关(图3g)。因此,间充质亚型中T细胞比例较高主要是由于巨噬细胞的浸润。
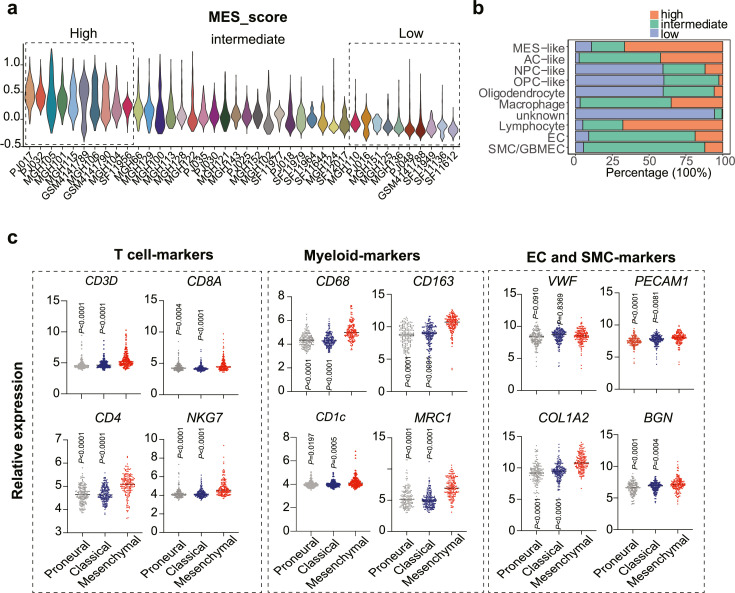

图3 PN-和MES-GBM的肿瘤免疫微环境解析
4、源自巨噬细胞的GPNMB有助于PN-MES细胞状态转变
利用NicheNet分析肿瘤微环境中的细胞间信号通讯,鉴定到了多个基质细胞-肿瘤细胞相互调控的配体-受体对,其中预测到巨噬细胞高表达的GPNMB与大多数间充质靶标存在相互作用(图4a),GPNMB是一种跨膜糖蛋白,最初是在肿瘤细胞中发现的,参与肿瘤迁移、侵袭、转移,通过直接抑制T细胞活化来逃避免疫;Tips:基于个性化分析结果,优先筛选TOP基因(显著性、差异倍数、靶标基因数目等),结合研究领域内已有特定功能报道的基因或通路,可以帮助更快锁定目标分子。
HPA和TCGA数据分析结果显示,GPNMB主要在巨噬细胞中表达,并且与巨噬细胞标志物显著正相关,这表明巨噬细胞是GPNMB的主要来源(图4b, c),流式细胞术结果证实了GPNMB主要在巨噬细胞上表达,而不是树突状或肿瘤细胞。Tips:流式细胞术是单细胞测序常见的下游验证方法,可用来分选目标细胞类群、验证细胞比例的变化和新鉴定的maker基因作为特定细胞分选的可行性等。
GPNMB在MES亚型患者中高表达,并且与低级别和高级别胶质瘤的预后不良相关(图4d, e);推测高表达GPNMB的巨噬细胞可以诱导肿瘤细胞向MES表型转变,进一步利用细胞共培养系统来验证这一假设,结果表明,长期接触巨噬细胞可以诱导肿瘤细胞中间充质转录因子的表达,并且靶向GPNMB的中和抗体治疗可以部分消除这种作用,表明GPNMB是PN-MES状态过渡的重要调节因子(图4f)。
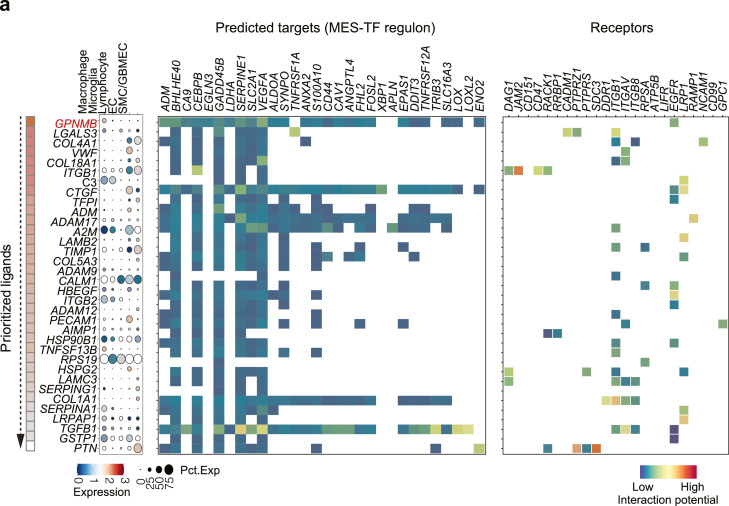
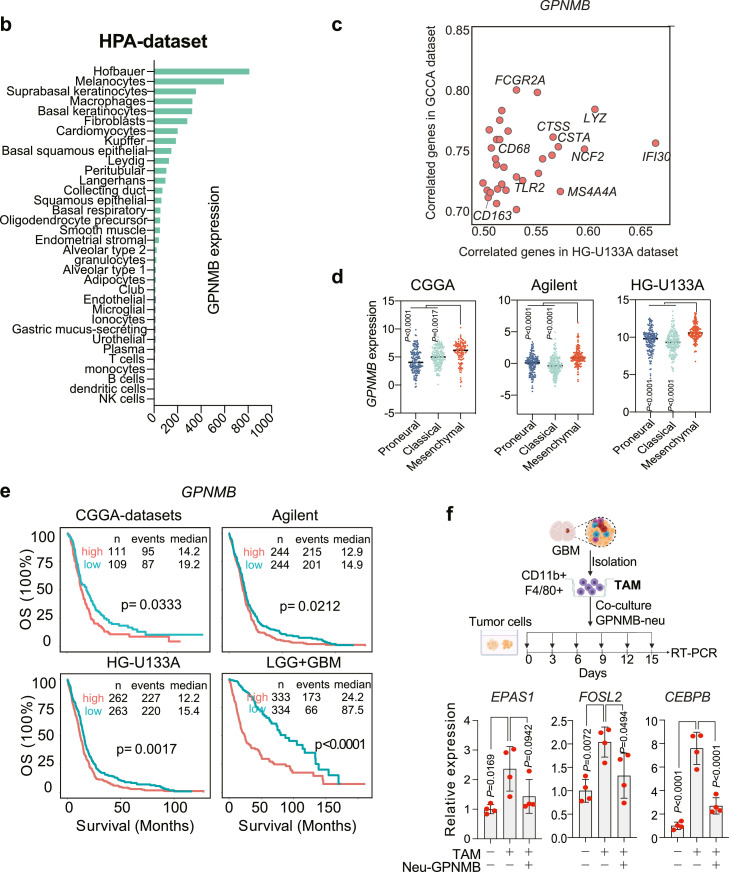
图4 源自巨噬细胞的GPNMB有助于PN-MES细胞状态转变
5、小鼠scRNA-seq分析单核细胞分化为Gpnmb-high巨噬细胞
收集小鼠GBM scRNA-seq数据,重点关注在早期(d7)和晚期(d28)GBM小鼠的CD45 +免疫细胞。根据细胞maker基因表达鉴定到了NK cells、Cd8+ T cells、Cd4+ T cells、 B cells、neutrophils、cDC1、cDC2、pDC、mDC、monocytes、TAM、monocytes/TAM、microglia cells(图5a);与以往的报道类似,巨噬细胞随着肿瘤进展急剧侵入肿瘤部位,而小胶质细胞在肿瘤发展过程中逐渐消失(图5b);细胞轨迹分析推断出树突状细胞和巨噬细胞起源于单核细胞,并随着肿瘤进展而逐渐分化(图5c);不同的通路主导了肿瘤浸润T细胞的募集,单核细胞主要表达Cxcl10、Cxcl9、树突状细胞特异性表达Ccl17、Ccl22,而巨噬细胞表达Ccl24,Saa3、Arg1和Gpnmb仅在巨噬细胞中出现(图5d);在肿瘤发生过程中,Arg1和Gpnmb的表达在巨噬细胞中被强烈诱导(图5e-g),这与人GBM数据集中的发现一致;然而,Gpnmb敲低后CD206(经典M2巨噬细胞标志物)表达不变,提示GPNMB不是M2巨噬细胞极化的驱动因素;免疫荧光染色显示GPNMB+巨噬细胞与T细胞共定位(图5h),表明它们之间存在潜在的相互作用。
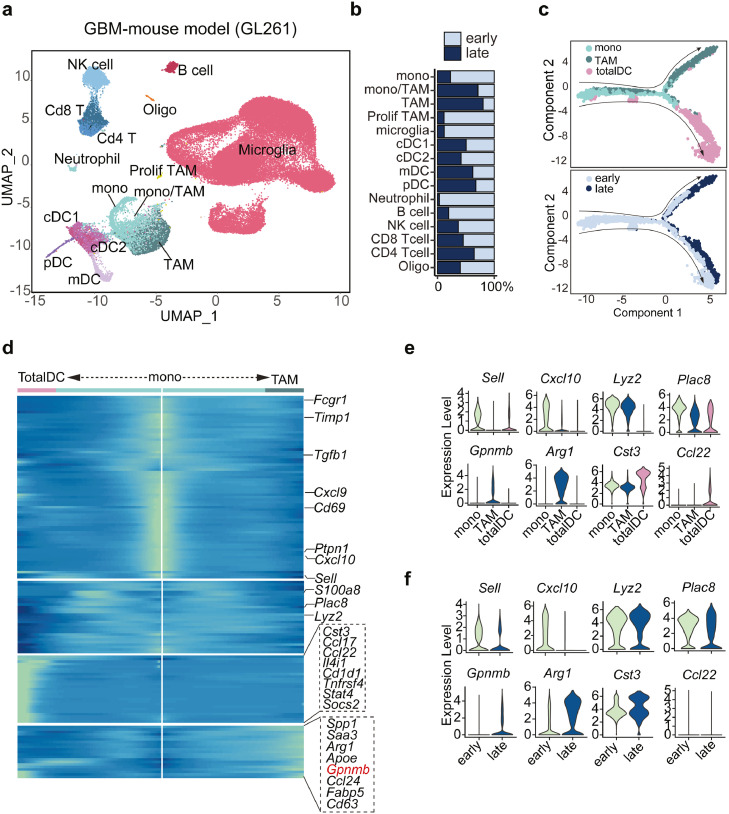
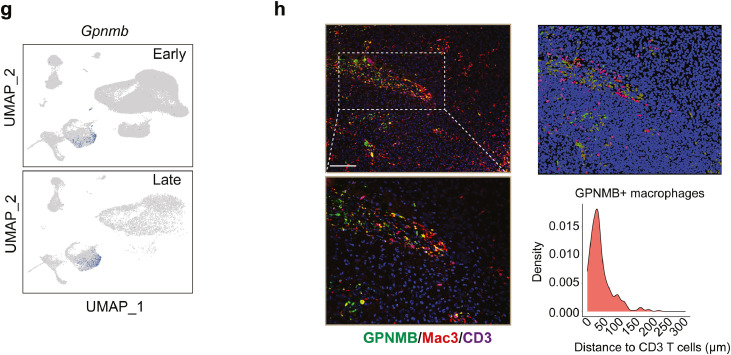
图5 小鼠scRNA-seq分析单核细胞分化为Gpnmb-high巨噬细胞
6、GPNMB-high巨噬细胞影响DC激活T细胞
利用CytoTalk算法分析GBM中T细胞与APC-like细胞间的相互作用,研究完整的信号转导途径,结果显示,T细胞通过Chemokines、cytokines、co-stimulatory/inhibitory、antigen-presentation通路与单核细胞、Gpnmb-high巨噬细胞、树突状细胞相互作用,并且DC细胞与Gpnmb-high巨噬细胞共享Cxcl16-Cxcr6趋化因子信号与T细胞相互作用。为了验证Gpnmb-high巨噬细胞的调控机制,从GBM肿瘤和正常小鼠中提取F4/80 + GPNMB +巨噬细胞、D11c + DC和骨髓来源的单核细胞,然后与na?ve T细胞共培养(图6e);实验结果显示,与GPNMB+巨噬细胞和单核细胞相比,CD11c + DC共培养表达更高水平的CD69、IFNγ和GZMB,能更好地诱导T细胞活化(图6f);T细胞增殖实验检测结果也表明,与GPNMB+巨噬细胞和单核细胞相比,CD11c + DC能显著促进T细胞增殖(图6g)。综合以上结果,确定了关键的GPNMB-high巨噬细胞亚群是GBM细胞间通讯的枢纽,不仅诱导PN-MES肿瘤细胞转化,而且通过与DC竞争而损害T细胞激活。Tips:利用细胞通讯分析筛选潜在细胞间互作的受体-配体对,结合细胞共培养、co-IP和免疫荧光等实验,可以探究目标细胞类型对特定细胞功能的影响及机制。
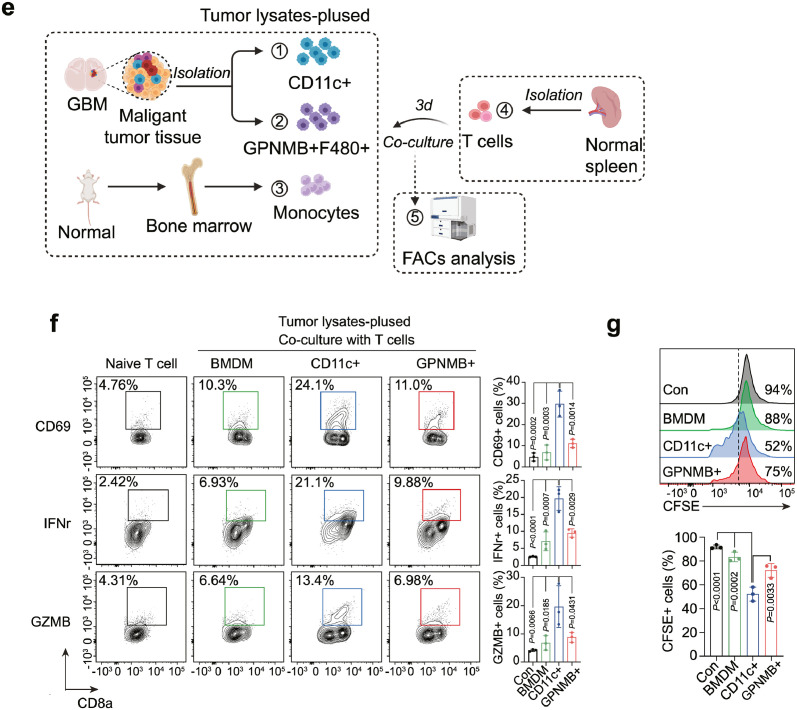
图6 GPNMB-high巨噬细胞影响DC激活T细胞
研究总结
1、本文通过scRNA-seq数据将高度异质性的GBM肿瘤细胞分为MES-like、AC-like,OPC-like和NPC-like亚型;
2、利用细胞轨迹分析和转录调控网络分析预测到由特定TF调节的PN到MES细胞状态转换;
3、利用空间转录组数据、TCGA数据库、细胞通讯分析,锁定到了关键的GPNMB-high巨噬细胞,在PN-MES细胞状态转变中发挥重要作用;
4、通过信号转导分析和细胞共培养研究,进一步揭示了这些源自单核细胞的GPNMB高巨噬细胞亚群可能无效地保留T细胞不被树突状细胞激活,提示未来靶向GPNMB-high巨噬细胞的联合免疫治疗可作为有潜力的治疗策略。
如果您对该研究思路感兴趣,欢迎点击下方按钮联系我们,我们将免费为您设计文章思路
参考文献
Xiong A, Zhang J, Chen Y, Zhang Y, Yang F. Integrated single-cell transcriptomic analyses reveal that GPNMB-high macrophages promote PN-MES transition and impede T cell activation in GBM. EBioMedicine. 2022;83:104239. doi:10.1016/j.ebiom.2022.104239








 京公网安备 11011302003368号
京公网安备 11011302003368号