PCR(polymerase chain reaction)扩增目的片段→电泳(electrophoresis)→纯化(purification)→连接 (ligase )→转化(transformation)→阳性克隆(positive clone)→检测(detection)
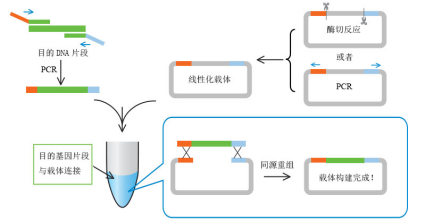
图1:无缝克隆流程图(图片来源于网络)
2. PCR扩增:选择要扩增的目的片段,在正义链和反义链的末端分别设计一条带有线性化载体正义链和反义链部分同源序列一致的引物,此处参考说明书建议(15-25bp)。为了减少非特异性扩增,建议与靶序列的匹配度越高越好。
3.电泳:PCR结果的好坏通常通过琼脂糖凝胶电泳来观察条带有无或者浓度大小,基本原理是琼脂糖凝胶介质中添加了在紫外下可以显色的EB, 这种试剂可以嵌合到核酸分子中,与DNA双链结合,因此,分子量越大的DNA分子,显色度越高,在相同浓度下也越亮。有的时候如果分子量很小的DNA, 浓度又不高的情况下,DNA条带有可能会出现假阴性的结果。
4.目的片段的纯化(胶回收):PCR扩增结束后,体系中可能会有未参与反应的聚合酶,Mg2+等,所以一般是建议通过纯化的步骤将这些杂质去除,以利于后续反应的稳定进行。
载体线性化:目的片段插入需要将环状的质粒用酶来消化成线性的双链DNA分子,实际情况下载体消化会因为反应时间和酶量多少而有较大区别,如果用于后续的基因克隆,建议消化尽量完全。
5.连接反应:Biomarker MultiF Seamless Assembly Mix试剂盒可以将多个片段组合到载体上,形成一个环状的重组质粒。用于后续的建库测序或者诱导蛋白表达。
6.转化:基本原理是质粒容易在大肠杆菌中稳定繁殖,这部分是基因克隆的关键,如果成功,后续的平板上会有单克隆的出现。有单克隆出现可以进行下一步实验。单克隆平板可以在4 ℃冰箱存放一个月,仍然不失效。
7.检测:挑取带有抗生素平板单克隆扩大培养,3-4 h, 使质粒拷贝数增加,随后用于菌落PCR检测,是否是插入了目标片段的质粒。
小贴士
其他判断阳性单克隆的方法?
最可靠的方法是酶切,一个环状重组质粒,在对应的位置用限制性内切酶双酶切后,会出现两个目的片段,如果不能出现两个片段,一般可以认为是空载体没有线性消化完全。
结果展示
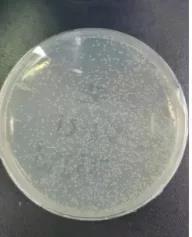
图2:单克隆检测示意图
结果分析
携带有目的片段的质粒能够抵抗抗生素,才使得在平板培养基上长出来。但也有可能是没有消化完全的空质粒。因此,下一步的鉴定实验显得尤为重要。菌落PCR在分子生物学实验中,容易有假阳性出现,可能的原因很多,因此,最根本的方法就是提高阳性率。以质粒为模板扩增,产物浓度会很高,可作为判定假阳性的一个依据。以及上述所提及的质粒的酶切,都是最常用的方法。
保存条件
产品应用
DNA定点突变
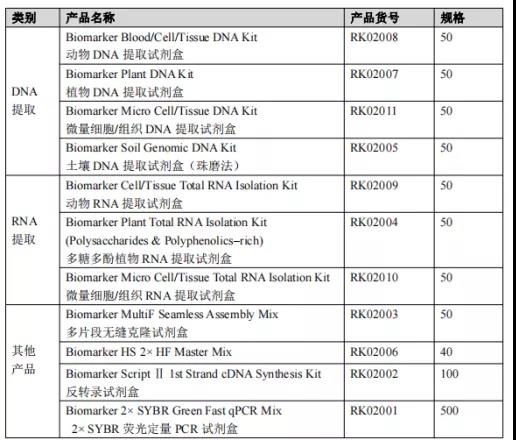
相关产品








 京公网安备 11011302003368号
京公网安备 11011302003368号