
膀胱癌患者接受免疫治疗后预后效果的好坏仍然是临床上面临的一个主要的挑战。近期NC一篇文章通过单细转录组及空间转录组阐述了对膀胱癌治疗具有反应应答的癌细胞群。获得了在预测对免疫治疗的反应方面更优的marker基因。有助于为患者的治疗提供更理想更优的治疗方案。
百迈客不仅提供单细胞系列产品,6大核心产品,单细胞转录组、空间转录组、单细胞免疫组库、单细胞ATAC-seq、单细胞核转录组、单细胞全长转录组,而且实现了单细胞转录组、空间转录组百迈客云端APP分析,深入大数据挖掘,一键快速分析,单细胞和空间转录组的联合分析近似实现单细胞分辨率的空间异质性,助您进入时空组学研究新时代。
摘要
术前新辅助化疗(NAC)和免疫检查点治疗(ICT)已经彻底改变了膀胱癌的治疗。然而,从这些模式中获益最多的患者分层仍然是一个主要的临床挑战。作者将人类膀胱癌的单细胞核转录组、空间转录组和单细胞分辨率的空间蛋白组联合分析,确定具有治疗反应预测能力的上皮细胞亚群。这些细胞表达Cadherin12(CDH12,N-Cadherin 2?)、catenins和其他上皮细胞的标志物。CDH12富集的肿瘤可以定义患者是否接受NAC治疗后预后效果差。富集CDH12的肿瘤对ICT表现出更好的效果。在所有情况下,通过对肿瘤CDH12富集进行患者分层比目前膀胱癌亚型能更好的预后预测。CDH12群体类似于一种未分化的状态,具有固有的侵略性生态学,包括化学耐药性可能是通过祖细胞样基因表达和成纤维细胞激活介导的。CDH12富集细胞表达PD-L1和PD-L2以及耗竭T细胞共定位,可能通过CD49a(ITGA1)介导,为ICT在肿瘤中的功效提供一种解释。总之,本研究描述了一个对膀胱癌治疗具有反向应答的癌细胞群。重要的是还为临床标志物的筛选提供了一个令人信服的框架。
研究背景
肌肉浸润性膀胱癌(MIBC)的分子分型改变了目前关于MIBC发病机制的概念。然而,即使是最近达成共识的分子分类系统也没有为其在临床决策中的应用提供令人信服的证据,特别是缺乏对治疗反应的预测。利用单细胞RNA测序分析MIBC的新兴研究为肿瘤内异质性提供了初步认识。然而,这些研究主要集中于肿瘤微环境,受限于相对较小的队列规模,尚未提供一个更明确的治疗决策途径。在单细胞水平上的MIBC上皮和非上皮细胞的全面分析将有助于将当前的分子亚型解转到它们的组成部分,从而开发出更有效的预后和预测工具。
材料方法
试验材料:25例MIBC患者和4例非膀胱癌对照的尿路上皮组织
试验方法:sn-RNAseq、空间转录组、TCGA数据库bulk数据、免疫组化
研究结果
1、表达CDH12上皮细胞的鉴定
为了实现表征肿瘤内异质性的第一个目标,作者首先基于sn-RNAseq细胞类型比例研究了MIBC肿瘤的总体细胞组成(图1a)。肿瘤由约90%的上皮细胞、5%的免疫细胞、3%的成纤维细胞和2%的内皮细胞组成,这些细胞根据相应的角蛋白、PTPRC、胶原蛋白、PECAM1、VWF等关键标记基因(图1b)。上皮间室无监督聚类识别到了一个KRT13和KRT17差异表达的类群,KRT13、uroplakins(UPK)、KRT6A细胞周期相关基因类群,以及表达CDH12和其他上皮标记物的细胞群(图1d)。KRT13和UPK人群是仅有的两个缺乏来自免疫浸润MIBC的基因标记的人群,这表明在这些人群中富集的肿瘤代表免疫“冷”肿瘤(图1e)。进一步交叉参照传统的尿上皮分化相关标记表明,KRT13和UPK群体代表一个更分化的表型,而CDH12、KRT6A和cycle群体代表一个未分化或去分化的表型(图1f)。如预期一样KRT13和UPK群体表达了一个上皮细胞分化网络(图1g)。基于单细胞调控网络推断和聚类分析,预测CDH12群体表现出多种发育相关转录因子的高活性,包括NANOG、EOMES、PAX1和HOXD9(图1h)。CDH12和循环群体在干-样和神经内分泌基因标签得分也高(图1i)。

图1?单细胞核转录组发现CDH12+肿瘤细胞群
2、在健康正常的膀胱上皮细胞中可以发现富集CDH12的细胞
上皮细胞的无监督聚类分为基础、过渡和伞部类群(图2a)。有趣的是CDH12群体与后一类典型群体明显不同,而过渡群体的KRT13和KRT17表达水平最高(图2b)。确定了一个始于基础细胞的轨迹,随后分化为两种途径:一种贯穿CDH12群体,一种跳过CDH12群体(图2c和d)。关键的尿上皮分化标记物沿着这条路径跟踪,在起始阶段CD44高表达,随后中间是KRT13和KRT17,终点站为UPK1A、GATA3、PPARG(图2e)。所有4个正常样本的拟时序分析显示出相似的路径,CDH12群位于起始点附近(图2f)。为了确定CDH12肿瘤细胞与正常肿瘤细胞之间的转录相似性,并推断它们在正常上皮细胞分化轨迹上的位置,作者使用表达相似性,确定了每个MIBC上皮细胞中最接近的正常细胞,然后给肿瘤细胞分配相应的正常潜伏期(图2f)。值得注意的是,最未分化表型对应的间隔得分预测了较差的疾病特异性生存(DSS),而最分化表型对应的间隔得分预测了较好的DSS,中间的间隔得分显示了相反结果之间的过渡(图2f)。
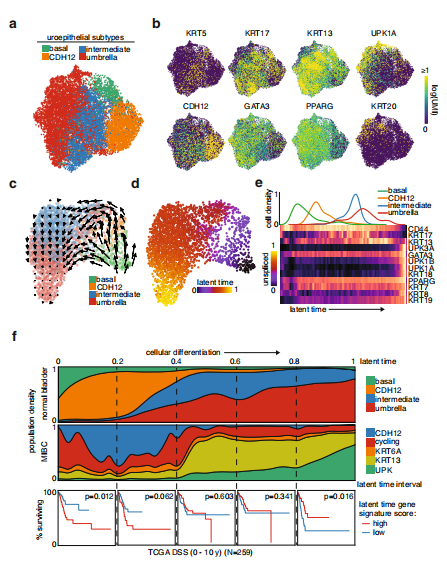
图2 CDH12+肿瘤群体类似于早期未分化尿路上皮细胞的特征并与较差的临床结果相关
3、CDH12评分预测MIBC患者不良预后

图3?高CDH12评分预测化学耐药性和成纤维细胞活化
4、CDH12评分预测对新辅助化疗的不良反应
5、CDH12细胞具有耐化疗性并能激活基质
6、CDH12评分预测化疗后免疫治疗反应
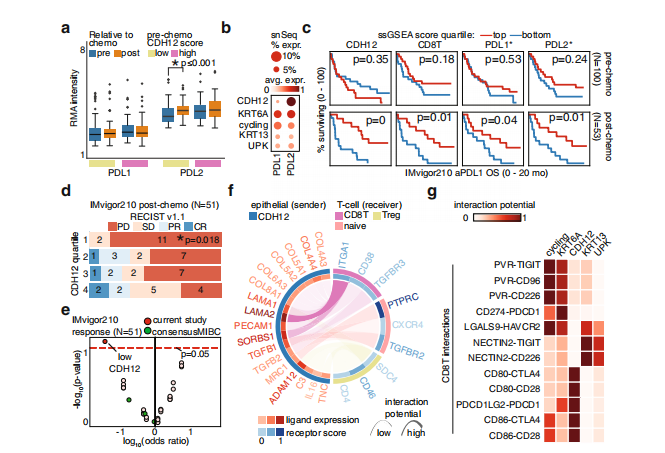
图4化疗后CDH12评分预测免疫检查点治疗的良好反应
7、CDH12细胞通过CD49a和CD8 T细胞相互作用
8、CDH12细胞与CD8 T细胞共定位
为了验证CDH12上皮细胞引起T细胞假说,作者使用Visium空间转录组和单细胞核转录组研究肿瘤中基因表达定位。CDH12富集的区域也富集了CD8T细胞marker和ITGA1(图5a)。为了验证CDH12上皮细胞在单细胞水平上与T细胞共定位,作者设计并使用CODEX平台对同一肿瘤队列的肿瘤组织微阵列进行了35位免疫组化检测(图5b)。

图5 CDH12肿瘤细胞优先与表达CD49a、PD-1和LAG3的T细胞共定位
9、CDH12细胞用耗竭的CD8 T细胞定义细胞生态位
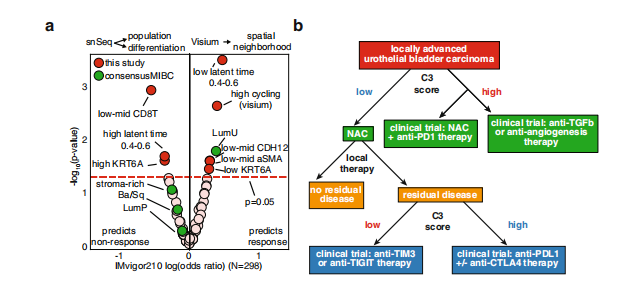
研究结论








 京公网安备 11011302003368号
京公网安备 11011302003368号