
发表期刊:Journal of Hazardous Materials IF:14.224
发表时间:2022.09.16
研究背景
环境中细菌的抗生素耐药性由于与临床病原体的抗生素耐药性密切相关而受到越来越多的关注。自从人类在临床上使用抗生素以来,环境中的抗生素耐药基因(ARGs)亦有所增加。然而,这种增加是否直接来源于环境残留抗生素的选择性压力还是来源于人类大量排放的粪便污染却不得而知。在该项研究中,调查了人类粪便以及受人类粪便污染影响的不同污水处理厂受纳水环境中的 ARGs、crAssphage 和抗生素残留特征,以期了解抗生素的选择压力和人类粪便污染对受纳水体ARGs污染的影响。
技术路线
主要结果
1.人类粪便和水环境中 ARGs 的污染特征
运用高通量qPCR方法从采集的样本中检测到89个ARGs和5个MGEs。在所有检的基因中,只有超广谱β-内酰胺酶编码基因blaTEM在所有样本中都被检测到。在>80%的样品中检测到strB、ermF、aadA1等ARGs(图1A)。在所有采集的人粪便中检测到28种ARGs,包括tetW、 cfxA、 tetO-01、tet(32)、blaTEM-1等,而在所有水样中仅检测到strB和blaTEM-1(图2)。此外,比较了不同的环境,发现在人类粪便和水中检测到38个ARGs(图3S1B)。总体而言,人粪便的ARG相对丰度显著高于所有水样。

图1.不同样品间ARG丰度和多样性的比较。(A)ARG相对丰度热图。深蓝(ND)表示结果低于检测限;(B)ARG的总相对丰度;(C)ARG的香农多样性指数;(D)不同样品中ARG组成的主坐标分析(PCoA)。
ARG多样性也随着水从污水处理厂向自来水的输送而减少(1C)。所有样本的ARG谱的PCoA表明,不同类型的样本包含显著不同的ARG成分。从环境样品中分离出人类粪便中的ARGs(图1D),表明肠道具有独特的ARG图谱。这可能是因为与环境相比,肠道的条件不同。来自污水处理厂和受纳河水的样品聚在一起较近,证实了污水处理厂出水的排放对受纳河中的ARGs有很大影响。同样,湖泊和自来水更倾向于聚集在一起,与所研究的湖泊都是自来水水源一致。上述结果表明,在所研究的样品中普遍存在ARGs,污水处理厂携带的ARGs可能污染不同的受纳水体。
2.人类粪便污染对水环境中 ARGs 的贡献
借助人类粪便指示剂 crAssphage (CPQ_056),分析了人类粪便排放对当地水环境中ARGs的影响。结果表明,crAssphage在所有环境样品中的检测频率为 68.2%,相对丰度范围为2.68×10-6至1.96×10-2每个16S rRNA基因拷贝(图2),表明超过一半的水样(湖水、自来水、污水处理厂和受纳河水)被人类粪便污染。与 ARGs 一致,平均crAssphage 丰度也沿着水流从污水处理厂不同处理单元的污水到受纳河水再到湖泊水体的顺序逐渐减少(图2)。这再次证明了人类粪便污染从污水处理厂的排放源到接收环境有着随距离不断衰减的效应。
进一步的统计分析探讨粪便污染对不同水体中 ARGs 的影响。Spearman相关性分析表明,总ARG相对丰度与crAssphage的丰度呈正相关(图3A)。进一步分析表明,crAssphage 丰度同样与某些 ARG 的丰度显着相关,例如氨基糖苷类、FCA、MLSB、其他/外排、四环素和磺胺抗性基因(图3B-F,表S5)。14 种ARG亚型和ermF与 crAssphage 显着相关。更重要的是,这些 ARGs 亚型也同时在人类和水环境中检出,表明它们可能源自人类粪便并被输送到受纳水体。
此外,人类粪便样本中ARGs丰度与 crAssphage丰度之间没有相关性,证实了肠道里 ARGs 丰度与crAssphage 丰度无关。这对 crAssphage作为人类粪便污染的指示基因至关重要。因此,上述环境样本中ARGs 与 crAssphage 丰度之间的显着正相关表明供试受纳水体中 ARGs 的富集在很大程度上可归因于人类粪便污染。
除了crAssphage 之外,研究者通过构建系统发育树分析了来自所有样品的氨苄青霉素抗性菌株中的 blaTEM-1基因序列(图4)。结果表明,来自四种环境样品(湖水、自来水、污水处理厂和受纳河水)的blaTEM-1与肠道样品的进化关系密切(图4)。该结果表明blaTEM-1可能通过污水排放在人类粪便和受纳水体之间进行传播。然而,需要进一步的研究来验证这些发现。
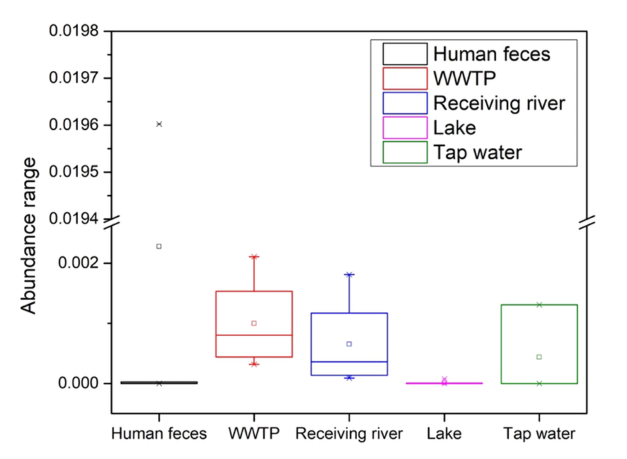
图2.不同类型样品中crAssphage的分布

图3.按目标抗生素分类的ARGs总丰度与水样中crAssphage丰度之间的相关性

图4.从不同样本分离的菌株中blaTEM-1基因的进化分析。样本根据类型进行着色。
3.水环境中的 ARGs 丰度与抗生素残留无关
研究者进一步测量了抗生素残留,结果表明,在所有五组中均检测到四环素类、喹诺酮类和硝基呋喃类抗生素。污水处理厂样品中17种抗生素的检出频率高于其他组,占 41.2%~64.7%。同时,在水环境中,污水处理厂的抗生素总浓度也高(289.5±236.7 ng/L),其次是受纳河水(169.8±104.9 ng/L)。自来水在所有样品中的抗生素残留浓度低 (54.7 ± 51.0 ng/L)(表1)。人类粪便中的总抗生素浓度为 17.7±9.2 ng/g。由于粪便提供者在过去六个月内都没有用药史,因此在人类粪便中检测到的抗生素可能来自饮用水或食物。此外,在所研究的人类粪便中检测到某些合成兽用抗生素,如磺胺氯哒嗪和恩诺沙星,也支持了这一结论。对水生环境中残留的抗生素和 ARGs 进行了相关性分析。与 crAssphage 不同,抗生素浓度与 ARG 丰度之间没有相关性。这一结果表明抗生素的选择并不能主要解释供试水环境中 ARGs 的丰度。综上所述,ARGs 和抗生素之间没有相关性,但却显著相关于crAssphage丰度,表明供试受纳水体中 ARGs 的丰度在很大程度上可以用人类粪便污染的程度来解释,本研究并没有观察到明显的抗生素选择ARGs现象。
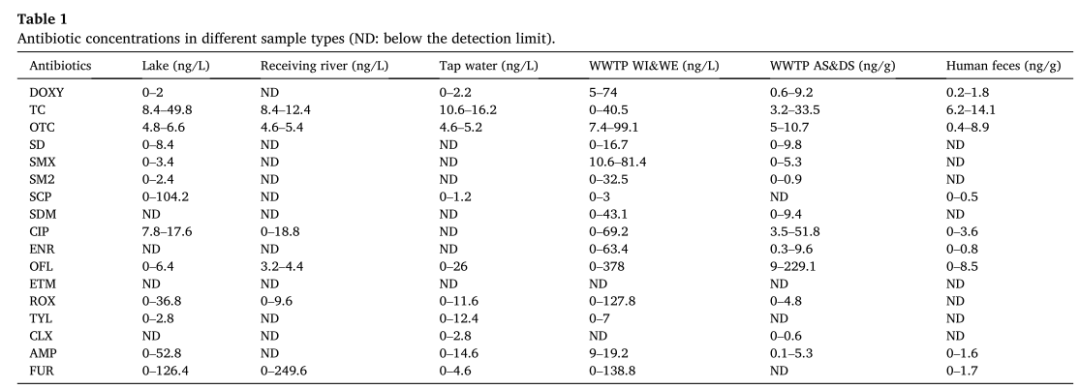
表1.不同样品类型中的抗生素浓度(ND:低于检测限值)。
4.细菌群落特征及其与ARGs的相关性
在人类粪便中,厚壁菌门、拟杆菌门、变形杆菌门和放线菌门是优势门(图5A)。厚壁菌和拟杆菌占肠道菌群总数的(83.5±9.8)%,环境样品中以变形杆菌和拟杆菌为主,变形杆菌所占比例高。在属的水平上,人类的肠道Bacteroides,Faecalibacterium,Bifidobacterium, 和Subdoligranulum.Pseudomonas,而水环境中的优势属为Flavobacterium,Arcobacter和Massilia(图5B)。
细菌群落多样性分析表明,除自来水外,其他水环境样品的平均Shannon指数均高于人类粪便样品(图5C)。PCoA分析表明,人类粪便和环境样本之间的细菌群落组成有显着差异(图5D)。然而,在人类粪便和水环境中存在着167个OTUS属121个常见细菌属,此外,还发现ARGs与所有样品中的细菌群落显著相关(图3A),这表明细菌群落组成决定了ARG组成,这一现象在各种环境中都被广泛观察到。
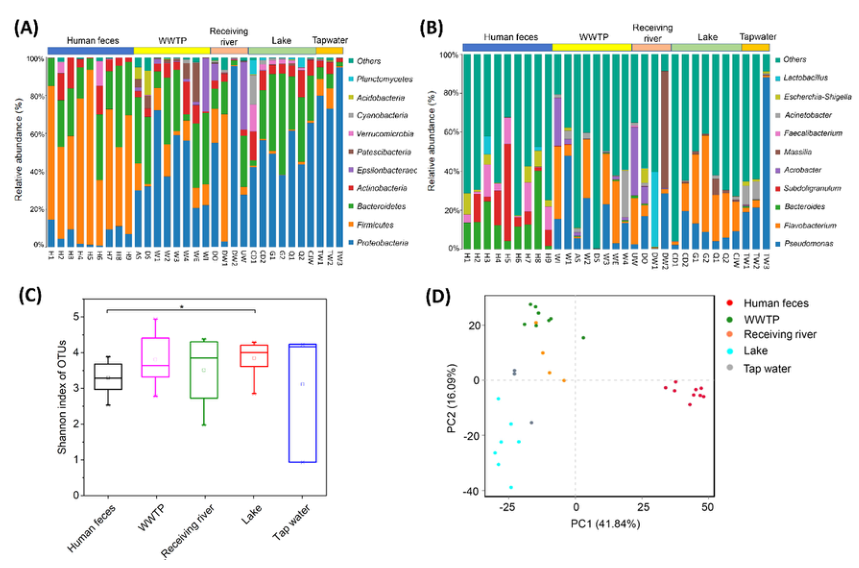
图5.不同样品中细菌群落的比较。(A)top10优势菌门的相对丰度;(B)top10优势菌属的相对丰度;(C)OTUs的Shannon指数;(D)OTUs的主坐标分析(PCoA)。
在该研究中,84个ARGs、5个MGES和20个细菌门被用来进行网络分析(图6B)。Chlamydiae和Dependentiae 与11种不同的ARG显著相关,表明它们的基因组中可能含有多种ARG类型。四环素耐药基因、大环内酯类耐药基因ermB和氨基糖苷类耐药基因aacA/aphD是四环素耐药基因的潜在宿主。Elusimmicrobia可能是aadE、blaCTX-M-02、Olec和vanRA-01的宿主。Synergistetes 可能是tetW、IS613和catA1的潜在宿主。由于该网络是建立在相关性的基础上,观察到的ARGs潜在细菌宿主仍需进一步的试验验证。
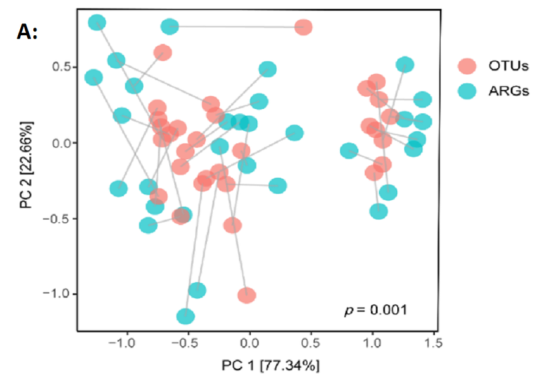
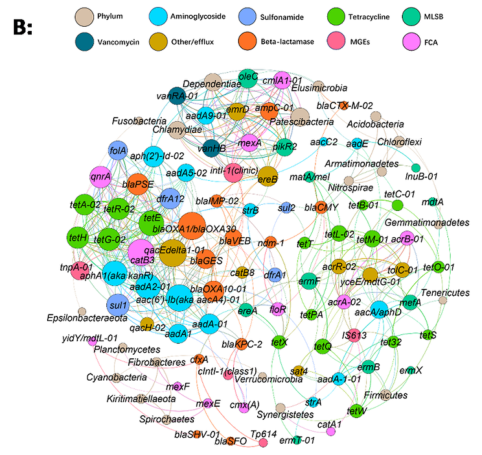
图6.不同样品中细菌群落与ARGs的相关性。(1)ARGs和细菌群落的Procrstes分析(2)细菌门和ARGs之间的网络分析
总结
这项研究主要表明,人类排泄物对受污水处理厂影响的受纳水体中的ARGs有显著的影响。ARG和crAssphage丰度都表现出从排放源到受纳水体的距离衰减效应。人类粪便中的blaTEM-1基因与水环境中的blaTEM-1基因具有密切的进化关系。在被人类粪便污染的环境中,粪便污染可能是ARG污染的主要来源。抗生素残留浓度与ARGs丰度之间无显著的相关性,表明环境残留抗生素选择产生ARGs的现象并不明显。该研究促进了公众对人类影响环境中人类粪便污染对抗生素耐药性的影响的理解。
百迈客微生物组学服务
百迈客生物在微生物领域深耕多年, 合作文章见刊于《Nature》、《Cell Host & Microbe》、《Water Research》、《Journal of Hazardous Materials》、《Environmental science & Technology》、《Bioresource Technology》等高水平杂志。百迈客可提供Illumina二代宏基因组、ONT三代宏基因组、PacBio全长微生物多样性、二代微生物多样性、微生物绝对定量等全套测序分析服务,项目经验丰富,累计处理样本数15万+,合作文章数600+,影响因子2500+,合作单位覆盖31个省及直辖市、400+家单位,百迈客致力于提供高质量的组学测序服务,欢迎点击下方按钮垂询!
参考文献
Chen Z, Duan Y, Yin L, et al. Unraveling the influence of human fecal pollution on antibiotic resistance gene levels in different receiving water bodies using crAssphage indicator gene[J]. Journal of Hazardous Materials, 2023, 442: 130005.
研究背景
非酒精性脂肪性肝病(NAFLD)已成为全世界关注的主要健康问题;它是一种主要的隐性疾病,会增加罹患多种慢性疾病的风险,如2型糖尿病和心血管疾病。NAFLD患者有发展为脂肪肝、肝硬化甚至肝细胞癌的风险。然而,NAFLD的诱导和进展的病理机制复杂,目前还没有明确的靶向药物。改变生活方式和改变饮食是目前缓解NAFLD的主要策略。因此,确定NAFLD的新靶点和治疗方法仍然是一个挑战。
NAFLD是由肝细胞内脂肪过度堆积引起的,新生脂肪生成是脂肪储存的重要途径。肝脏脂肪生成主要由固醇调控元件结合蛋白1 (Srebp1)调控,Srebp1增强脂肪生成基因的后续激活,包括脂肪酸合成酶(Fas)、乙酰辅酶a羧化酶(Acc)和硬脂酰辅酶a去饱和酶1 (Scd1),导致肝脏脂质积累。此外,NAFLD的发病和进展是众所周知的与炎症有关。肠道衍生毒素,如脂多糖(LPS),被认为在肝脏炎症中具有致病作用,并与NAFLD密切相关。一方面,有报道称LPS可促进Srebpl激活和肝脏脂质积聚。相反,LPS通过激活肝脏toll样受体4 (TLR4)/核因子-κB (NF-kB)信号通路触发炎症反应。
近年来,肠道菌群与NAFLD的关系引起了广泛关注。肠道微生物群产生促炎LPS并进一步影响肝脏脂质代谢,已成为NAFLD发展的重要参与者。研究表明,高脂肪饮食(HFD)喂养的无菌小鼠肝脏中的脂质水平低于传统饲养的小鼠。此外,将从高脂饮食诱导的肥胖供体中分离出的肠道微生物移植到无菌动物中,会导致受体小鼠体重显著增加和代谢综合征。因此,肠道菌群的稳态对维持健康至关重要,确定肠道菌群的组成对于研究NAFLD与失调之间的致病关系和潜在致病联系是必要的。
咖啡酸(CA),也被称为3,4 -二羟基肉桂酸,是最常见的酚酸之一,存在于大多数植物中,包括咖啡、水果和丹参。CA在人类饮食中广泛使用。越来越多的证据证实CA具有多种生物功能,包括抗氧化和抗炎活性。与此同时,据报道,CA减少alcohol-fed老鼠的肝脏脂质含量,抑制油的段脂肪生成人类HepG2细胞,和改善小鼠的肝脂肪变性和内质网应激通过增加自噬。然而,CA作用于脂质积累的机制尚不清楚。枸杞叶提取物含有多种酚酸,包括CA,有研究表明,枸杞叶提取物可以通过调节代谢谱和肠道菌群组成来改善大鼠2型糖尿病。然而,目前尚无关于CA对NAFLD肠道菌群影响的研究报道。本研究旨在探讨CA对NAFLD的降脂作用及其机制,尤其关注其对肠道菌群的影响。

英文名称: Caffeic acid prevents non-alcoholic fatty liver disease induced by a high-fat
diet through gut microbiota modulation in mice
中文名称:?咖啡酸通过调节小鼠肠道菌群预防由高脂肪饮食引起的非酒精性脂肪肝
杂??志:Food Research International
影响因子:5.0
材料方法
1、实验材料:
2、研究方法:
在ND适应1周后,将小鼠随机分为2组:ND组(n = 30)和HFD组(n = 30),治疗8周。
研究结果
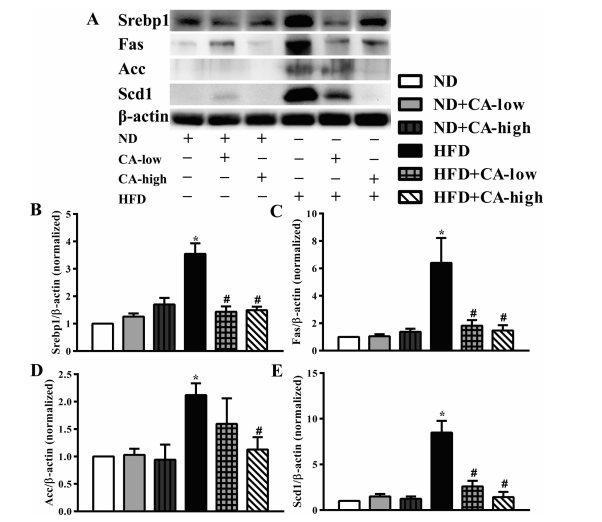
1.补充CA可降低高脂喂养小鼠的脂质积累
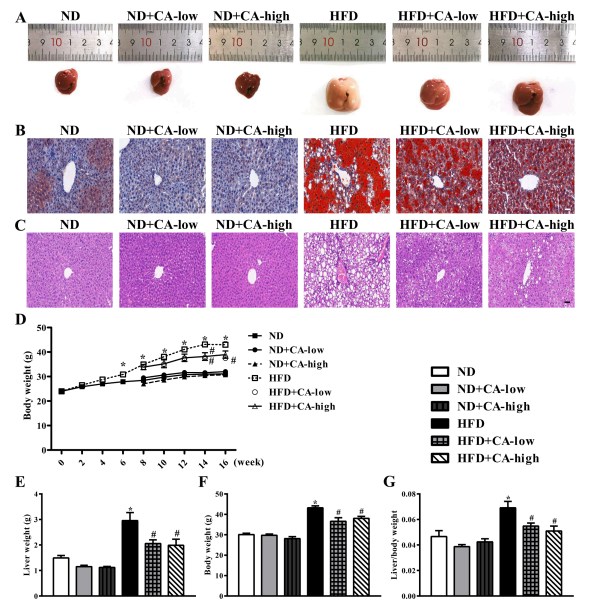
图1
2.CA的补充影响hfd喂养小鼠的生化标记物
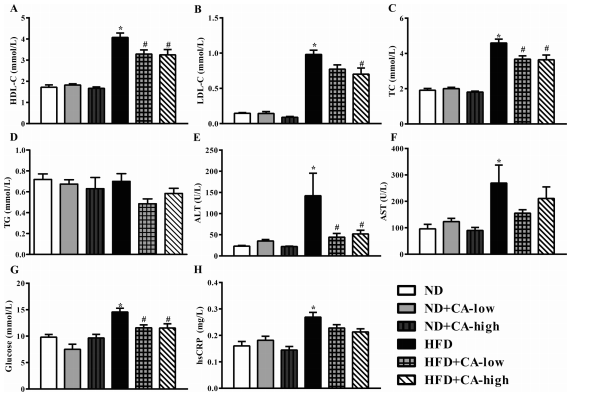 ? ? ?图2
? ? ?图2
 ?图 3
?图 3
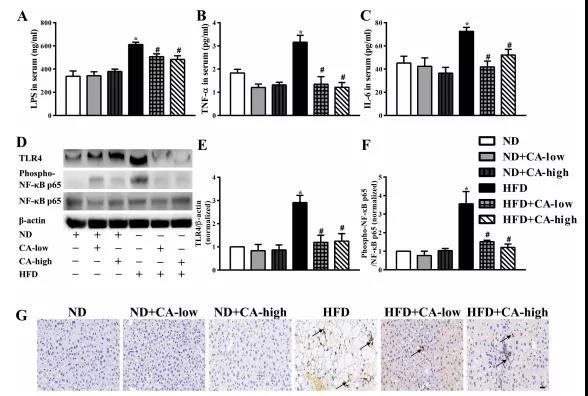
图4
5.补充CA可减少高脂饲料喂养小鼠的肠道菌群失调
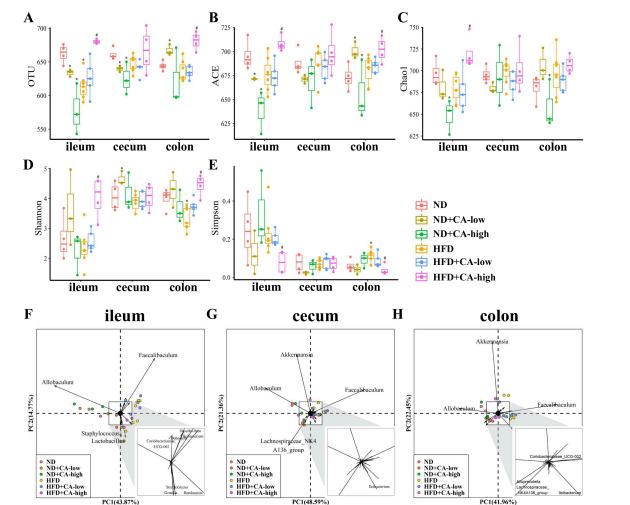 图5
图5
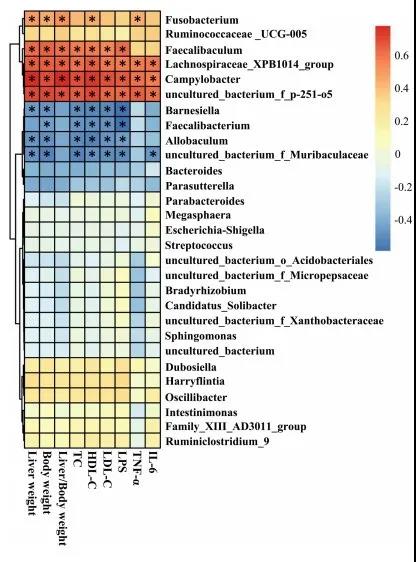
图6
7.结论
成功案例:谢黎炜团队利用机器学习算法在肠道菌群研究中取得新突破【成功案例】多组学研究套路之:微生物多样性16S测序+宿主转录组测序
签微生物组项目免费送培训班、送分析、享折扣!
【16S V4 16S全长微生物多样性测序】-完整的肠道微生物群可以保护遗传易感小鼠免受白血病的侵袭
非小细胞肺癌患者肠道微生物多样性预示ICI疗效
肠道微生物菌群多样性警示孕妇食用人造甜味剂的风险!
英文标题:Extract of the Microalga Nitzschia laevis Prevents High‐Fat‐Diet Induced Obesity in Mice by Modulating the Composition of Gut Microbiota
中文标题:菱形藻(Nitzschia laevis)通过调节肠道菌群来缓解高脂膳食引起的肥胖
发表时间:2018.12
期刊名称:Molecular nutrition & food research
影响因子:5.15
合作单位:北京大学?食品与生物资源工程研究所
研究背景
随着人类生活水平的提高,肥胖和超重人口越来越多,而人工合成药物(如褪黑素)的肥胖治疗往往会产生负面效应,因此,从自然界中提取成分“温和”的生物合成药物已经被人们广泛关注,近年来,以微藻为代表的海洋生物已成为研究的热点。研究表明,藻类中提取的辅助色素岩藻黄素能够通过抑制解偶联蛋白1(UCP1)调节脂肪组织的脂质代谢,岩藻黄素是一种四十二碳叶黄素,目前已被开发作为有效的减肥药。菱形藻(Nitzschia laevis)是一种富含岩藻黄素的硅藻,也是多酚和多不饱和脂肪酸(PUFAs)的主要来源,多酚和PUFAs能够调节肠道微生物的菌群结构和活性。研究发现,肥胖患者和正常人群的肠道微生物存在差异,因此推测,菱形藻中的提取物能够通过调节肠道微生物实现控制和治疗肥胖的效果。
材料方法
2. 试验对象:10周龄C57BL/6J小鼠。
3.?分组方式:①正常膳食组(NCD)、②高脂膳食组(HFD)、③高脂+低藻(10 mg/kg/d)膳食组(HFD-LE)、④高脂+高藻(50 mg/kg/d)膳食组(HFD-HE)。
4. 组织学分析(H&E):肩胛间的棕色脂肪组织(BAT)、白色脂肪组织(WAT)、附睾脂肪组织(epi-WAT)、肠系膜脂肪、腹沟股脂肪和腹膜后脂肪。
5. 生化分析:提取血清样本,检测总胆固醇(CHO)、总三酰甘油(TG)、低密度脂蛋白(LDL)和高密度脂蛋白(HDL)。
6. 蛋白印记分析(WB):紧密连接蛋白(ZO-1)、闭合蛋白。
7. 实时荧光定量PCR(RT-PCR):紧密连接蛋白(ZO-1)、闭合蛋白合成相关基因。
8. 肠道微生物多样性:粪便样本,16S rDNA V3-V4,Illumina Hiseq 2500,RDP数据库,PICRUST预测功能基因(KEGG、COG)。
重要结果与讨论
1. 菱形藻(Nitzschia laevis)对小鼠体重、脂肪厚度和肝脂肪的影响
水溶性化合物、类胡萝卜素、多酚和脂肪酸的比例分别为13.55%、7.27%、13.83%和7.3%,多不饱和脂肪酸(PUFA)占总脂肪酸的30.32%。NLE对HFD导致的小鼠体重增加的抑制具有剂量依赖性(图1B),NLE对HFD导致的小鼠体重增加的抑制作用不是通过抑制食物或能量摄入来实现的(图1C;?1D)。NLE能够降低HFD导致的脂肪厚度的增加(图1E-1G)。
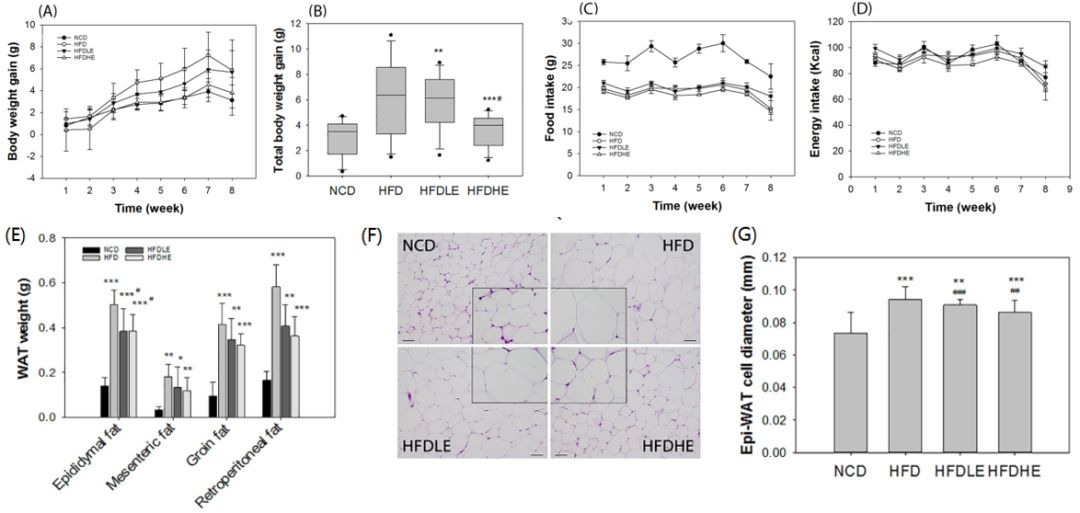
图1. A-D:小鼠的体重相关特征;E-G:NLE对小鼠的白色脂肪组织的影响
2.?菱形藻(Nitzschia laevis)对小鼠肝脏的病理影响
NLE未能显著降低HFD导致的BAT增长(图2A),与脂肪代谢有关的UCP1和PGC1基因表达在HFD-LE组中显著升高(图2C-2D),HFD-HE显著降低了肝重(图2E),NLE对HFD诱导的脂肪增生具有有效的抑制作用(图2F-2G)。Srebp1c与肝脂肪的变性有关,NLE对HFD导致的Srebp1c基因表达水平降低有恢复作用(图2H)。
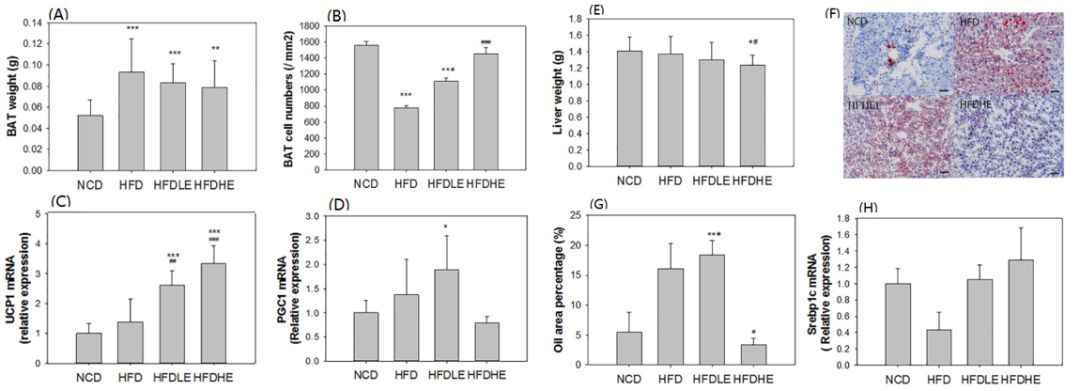
图2. A-D:NLE对小鼠的棕色脂肪组织的影响;E-H:NLE对小鼠肝脏脂肪变性的影响
3. 菱形藻(Nitzschia laevis)对小鼠血脂、胆固醇、血糖和肠上皮完整性的影响
HFD-LE组、HFD-HE组均未显著降低HFD导致的小鼠血清CHO、TG、LDL和HDL的升高(图3A-3D)。紧密连接蛋白(ZO-1)和闭合蛋白是肠道上皮和屏障功能完整的重要生物标志物,其表达的减少显著细胞外通透性增加。高浓度的NLE(HFD-HE组)显著恢复了HFD造成的闭合蛋白基因mRNA转录的降低(图3H)。NLE对闭合蛋白基因表达影响的剂量依赖性在West Blot试验中也有体现(图3I)。
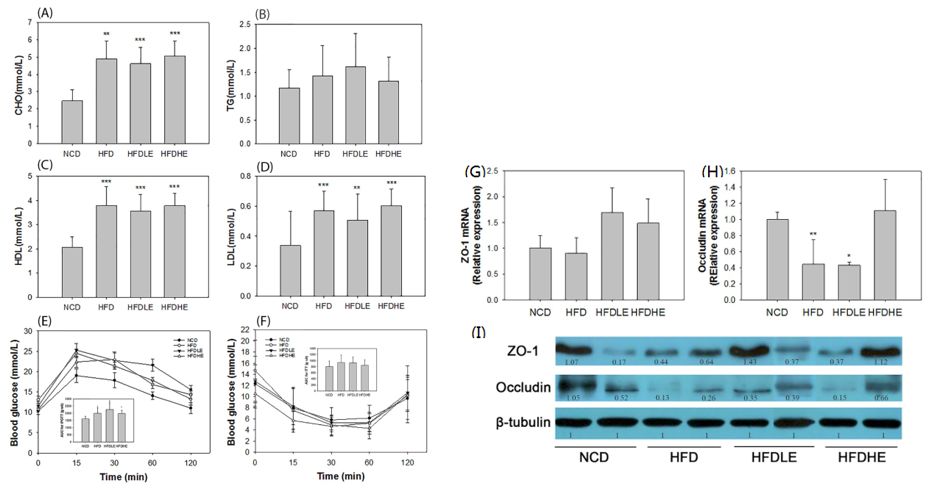
?图3. A-F:NLE对小鼠血脂、胆固醇、葡萄糖和胰岛素耐受性的影响;G-I:NLE对小鼠紧密连接蛋白(ZO-1)和闭合蛋白的影响
4. 菱形藻(Nitzschia laevis)对小鼠肠道微生物的影响
HFD导致小鼠肠道菌群的多样性降低,然而NLE恢复了菌群多样性(图4)。Proteobacteria?、Epsilonproteobacteria、Helicobacteraceae?和Campylobacterales在HFD-HE组显著富集(图5H;5I),NCD与HFD-HE组的菌群结构差异较小(图5J), NLE提高了HFD-HE和HFD-LE组Campylobacterales的丰度(图5K)。NLE恢复了部分HFD导致的[K]转录和[G]碳水化合物代谢与运输的功能类型(图5L)。
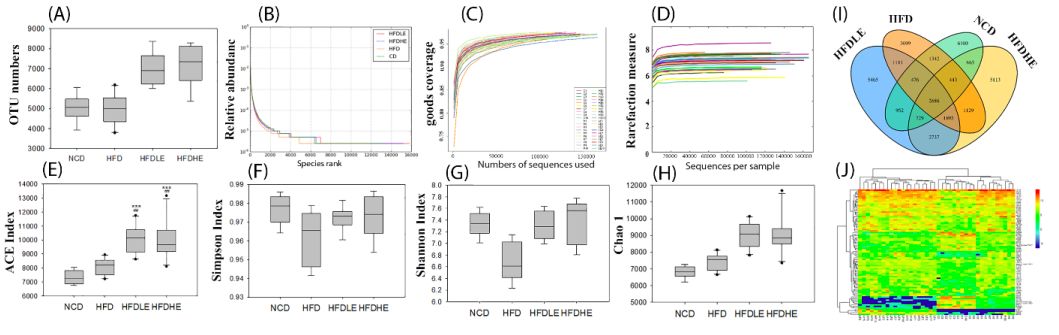
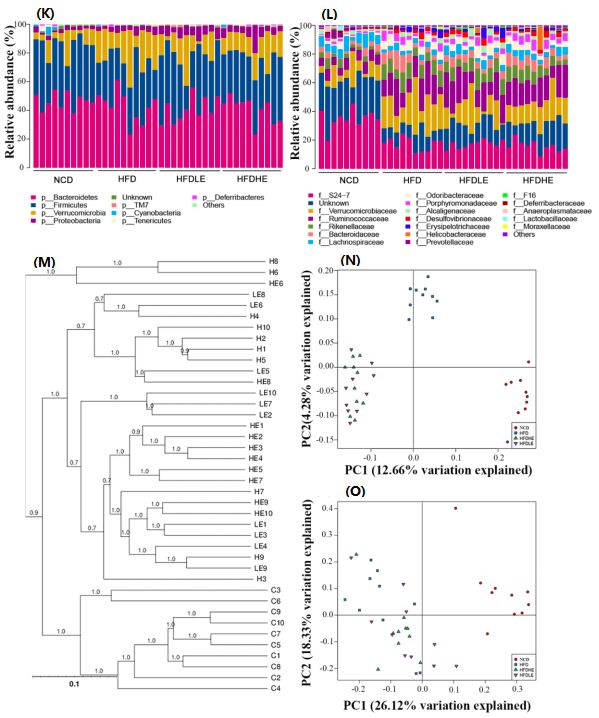
?图4.?NLE对小鼠肠道微生物α多样性(A-J)和菌群结构(K-O)的影响
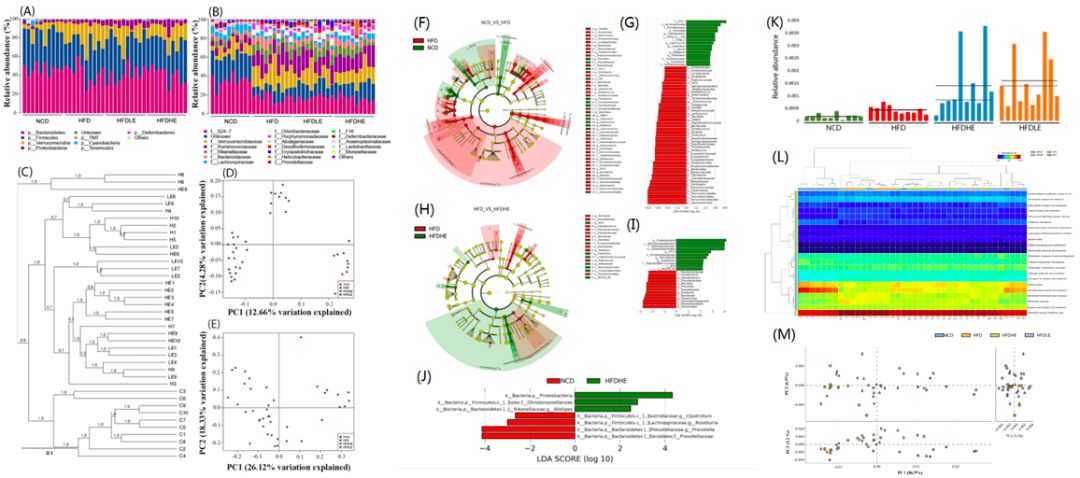
图5.?NLE对小鼠肠道微生物基因功能的影响
总结
菱形藻(Nitzschia laevis)能够有效地缓解高脂肪摄食(HFD)导致的肥胖症状,能够有效地恢复小鼠肠道微生物的结构和功能。
如果您的科研项目有问题,欢迎点击下方按钮咨询我们,我们将免费为您设计文章方案。
modulation?of?gut?microbiota?in?mice?
褪黑素通过调节小鼠肠道菌群预防肥胖
IF:9.314 期刊:Journal of Pineal Research
时间:2017.03 ?单位:北京师范大学 、百迈客生物科技
研究背景
肥胖是一个非常严重的健康威胁因素,在2014年全球体重超标的成年人达到20亿,其中至少有6亿是肥胖症。有大量研究表明肥胖是癌症和一些慢性疾病,如糖尿病、脂肪肝、心血管疾病等的风险因素。现如今肥胖已经超越吸烟,成为世界范围内最严重的健康威胁。目前研究表明肠道菌群失调会导致肥胖及其并发症的发生。已有研究揭示褪黑素可以促进体重的下降以及自身能量的平衡,但是褪黑素的益生作用是否与肠道微生态有关,目前尚未报导。而本研究发现,褪黑素是通过改变肠道微生物结构来预防肥胖及其并发疾病。
研究方法
小鼠随机分为3组,NCD(正常膳食)、HFD(高脂肪膳食)、HFD+M(高脂肪膳食+褪黑素)
Illumina?MiSeq;16S?rRNA?V3+V4;
组织学分析,生化分析,葡萄糖和胰岛素耐受分析,蛋白质印记分析。
研究成果
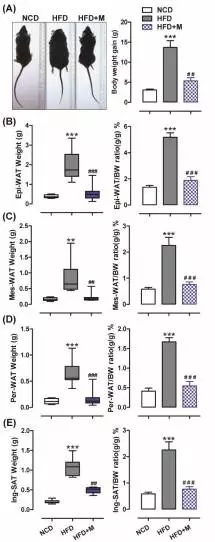
1,?褪黑素能显著地控制体重增加
1)?HFD组小鼠体重显著增加,而HFD+褪黑素组小鼠体重得到有效控制,如下图A。
2)分离小鼠四类主要的脂肪组织(Epi-WAT、Mes-WAT、Per-WAT、Ing-SAT),发现HFD显著促进这四类脂肪组织重量的增加,而褪黑素能有效抑制这四类脂肪组织重量的增加,如下图B-E。
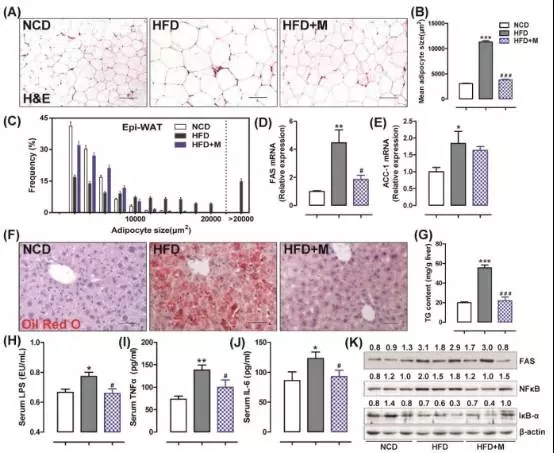
2,?褪黑素能控制白色脂肪组织,脂肪肝,系统性炎症
1)?通过比较Epi-WAT脂肪细胞的大小,发现HFD组脂肪细胞显著增大;而褪黑素通过减少>12000μm2的细胞数目,增加2000–8000μm2的细胞数目,使HFD+褪黑素组脂肪细胞大小维持在正常范围内,如下图A-C。
2)?通过比较Epi-WAT脂肪生成基因(FAS和ACC-1)的表达量,发现HFD显著促进FAS和ACC-1的表达,而褪黑素显著抑制FAS基因的表达,如下图D和E。
3)?通过观察油红O染色及比较肝脏TC含量,发现褪黑素能显著抑制肝脏内脂质积累,如下图F和G。
4)?通过比较血液内毒素(LPS)和炎症性细胞因子(TNFα和IL-6)的水平,发现褪黑素能显著抑制内毒素血症和系统性炎症的发生,如下图H-K。
3,?褪黑素能改善葡萄糖耐受性及胰岛素抗性
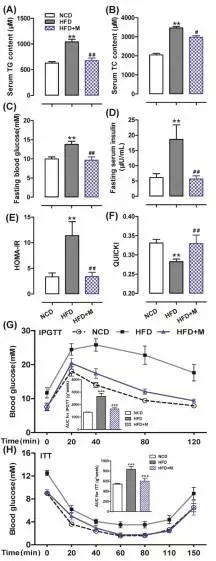
1)?通过比较血脂含量,发现HFD显著提高TG和TC含量,而褪黑素能显著降低TG和TC的含量,如下图A和B。
2)?通过比较血糖和胰岛素含量,并推导HOMA-IR和QUICKI指数,发现褪黑素能有效保护胰岛素敏感性,并且使血糖和胰岛素的含量发生颠倒,从而使HOMA-IR和QUICKI指数趋于正常水平,如下图C-F。
3)?通过葡萄糖耐受试验(IPGTT)和胰岛素耐受试验(ITT)分析,发现褪黑素能显著改善葡萄糖耐受性及胰岛素抗性,如下图G和H。
4,?褪黑素能促进棕色脂肪组织褐变及产热
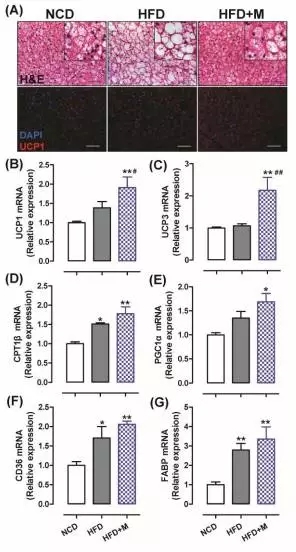
1)?通过棕色脂肪组织(BAT)石蜡切片分析,发现HFD促进脂质积累(切片白化),而褪黑素表现出相反的作用,并且褪黑素促进BAT中UCP1蛋白的表达,如下图A。
在BAT中,褪黑素显著增强产热基因UCP1和UCP3的表达,如下图B和C;线粒体生物合成基因PGC1α,脂肪酸分解代谢基因CPT1β,脂质转运基因CD36?和FABP的表达量也有提高,尽管未达到统计学的显著性,如下图D-G。
5,?褪黑激素改变肠道微生物结构
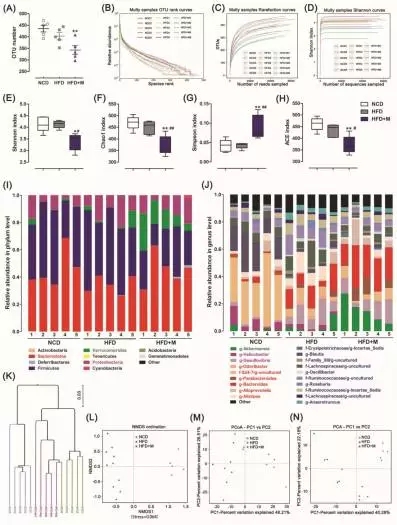
1)?通过对小鼠肠道菌群结构分析,发现褪黑素能显著降低OTU的数目以及微生物的丰富度和多样性,如下图A-H。
2)?门水平菌落结构分析,发现HFD显著降低拟杆菌门(Bacteroidetes)的相对丰度,而显著提高厚壁菌门(Firmicutes)的相对丰度。而褪黑素的加入会降低厚壁菌门/拟杆菌门的比例,并且会显著提高疣微菌门(verrucomicrobia)的相对丰度,如下图I。
3)?属水平菌落结构分析,发现褪黑素显著提高Akkermansia的相对丰度,Akkermansia属于疣微菌门(verrucomicrobia),如下图J。
4)?UPGMA、NMDS、PCA、PCoA分析,发现褪黑素显著改变了肠道菌群的结构,如下图K-N。
6,褪黑素能调节肠道菌群中的标志微生物
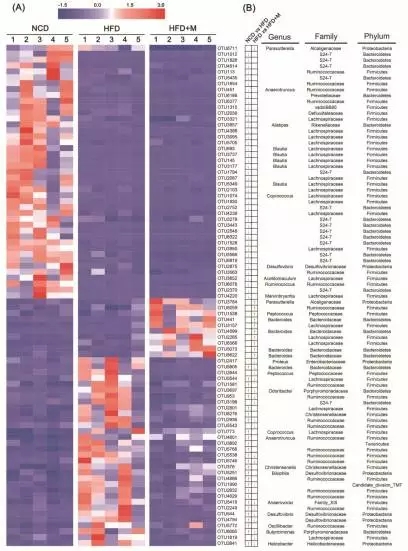
1) ?如下图显示,在三个分组中一共找到85个相对丰度有显著差异的OUT。与NCD组相比,HFD组有27个相对丰度显著增高的OTU,42个显著降低的OTU。与HFD组相比,添加了褪黑素的组有10个相对丰度显著增高的OTU,20个显著降低的OTU;而在这30个差异性的OTU中,有14个OTU的变化方向与和NCD组比较的结果完全相反。这14个OTU属于Ruminococcaceae、Desulfovibrionaceae、Bacteroides、Porphyromonadaceae、Helicobacteraceae、Christensenellaceae,有研究表明这些微生物与肥胖相关。
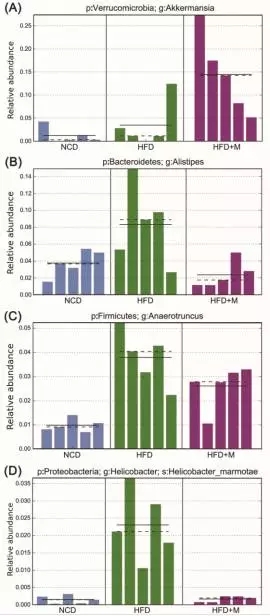
2) LEfSe分析,发现褪黑素显著提高Akkermansia的相对丰度,Akkermansia即是降低高脂肪膳食小鼠体重的有益菌。而褪黑素显著降低Alistipes、Anaerotruncus、Helicobacter?marmotae的相对丰度,则这三种细菌预防肥胖的有害菌。总之,褪黑素能够使高脂肪膳食小鼠的肠道菌群由失调状态转为正常状态,从而抑制体重的增加。
参考文献:
Xu?P,?Wang?J,?Hong?F,?et?al.?Melatonin?prevents?obesity?through?modulation?of?gut?microbiota?in?mice[J].?Journal?of?Pineal?Research,?2017.
]]>

